臨床試験
『植物性シリカ水溶液及び田七サポニン及びイノシトール配合品』の糖尿病患者への補助治療作用治験報告書
一般社団法人NSメディカル・ヘルスケアサービス
渡辺病院
鳥取大学医学部付属病院
大森内科クリニック
株式会社リージャ
他
序説
検体A(植物性シリカ〈もみ殻より抽出〉主成分とした水溶液にサポニン〈田七人参より抽出〉を配合及びイノシトール〈米糠より抽出〉を配合した液体)は、いずれも特殊な製法で採取される微量成分の一種であり製薬ではない。検体Aは、人間の自己免疫力を増強させ、抗病能力を高める働きを行い、且つ薬物治療をより効果的に発揮させ、病気を回復させる健康食品である。
日本国の一般社団法人クレディホールディングスは、多年にわたり植物性ケイ素の研究を実施してきた株式会社バイオシリカ研究所、京都大学農学部、その他研究機関の協力のもと、多大なノウハウを蓄積してきた。2013 年 6 月に我々は当該法人の委託を受け、検体Aを用いた糖尿病の補助治療の効果について 100 名に対する臨床試験を行った。以下にその臨床試験結果を報告する。
1.一般資料
被試験者のカルテはそれぞれ医療機関の問診及び一般財団法人メディカル・ヘルスケアサービスより提供された。検体B(治験者から採取した血液)は全部で 100 例あり、そのうち男性患者は 61 人、女性患者は 39 人である。年齢は最大 81 歳、最小 31 才であり、糖尿病の罹病(りびょう)期間は、2 ヶ月から 26 年まで違いがあった。他の病気との合併症としては、冠状動脈疾患 29 例、高血圧 23 例、脳血管疾患 22 例、腎臓病 8 例、末梢神経病変が 7 例であった。
2.試験方法
(1)被験者の選択
WHO の基準に従い、空腹時血糖値≧120mg/dl(6.7mmol/l)或いは、食後 2 時間経過後の静脈全血糖値≧180mg/dl(10.0mmol/l)を糖尿病の診断基準とした。Ⅰ型糖尿病が 5 例、Ⅱ型糖尿病が 95 例、合わせて 100 例を今回の観察病例として選んだ。
(2)試験方法
検体Aの臨床試験に参加した患者は、その観察期間においてそれまで継続して服用していた種々の薬の治療を維持し、それらの投薬品種、投薬時間、投薬方式及び投薬量は基本的に変更しない。同時に検体A投与期間には、患者の活動内容及び活動量も維持させ、食事の制限量も変化させない。精神的な刺激を避け、平静的な生活スタイルを保持することとした。
8 週間の試験を一つの治療プロセスとする。
(3)検体A投与方法
100 病例を 2 群に分けてもっとからだ天国を投与した。
第 1 群…
毎日起床時、朝、昼、夜の食間空腹時、就寝前に検体Aを 1.5cc から 1.75cc と飲料水 200cc を服用し、50 例を観察。
第 2 群…
毎日起床時、朝、昼、夜の食間空腹時、就寝前に検体Aを 3.0cc から 3.5cc と飲料水 200cc を服用し、50 例を観察。
(4)治療プロセス
8 週間を 1 治療プロセスとする。第 1 群は 1 プロセスを治療、観察。第 2 群は、2 プロセスを治療、観察。
(5)追跡観察組
連続 2 プロセスの治療、観察を受けた第 2 群の患者らを対象に、第 2 プロセスを完了した後、検体A天国を服用せずに 1 ヶ月経過した時点で、再び治療効果の評定を行う。
3.観察の内容
(1)その他の記載指示事項
検体Aを服用後の患者の自覚感覚についてはカルテに詳しく記載すること。
その他の例として多飲、多食、多尿、体力の変化、体重の増減及び他の合併症の変化など。検体Aの飲用によって発生した副作用、不良反応及び重要な体調変化をすべて詳細にわたり調査を行いカルテに記入する。
(2)生化学分析による検査内容
検体Aの服用前、服用後にそれぞれ肝機能、腎臓機能、グリコヘモグロビン(HbA1c)、血脂(コレステロール)値を検査する。静脈空腹血糖値を2週間に1回検査する。3 日毎に尿糖値を検査する。
体重を 2 週間毎に検査する。
(3)臨床資料の統計処理
各項目生化学指標の検査結果と患者自身の感覚の対照(t 統計 P<0.05 時差異が大とする)。
「参照値±標準値」で表示する。
4.観察結果
(1)治療効果の判定標準顕著な効果あり…
生化学的測定指標と患者自身の感覚共に大きな改善があった。
効果あり…
科学的測定指標の改善は大きくないが、患者自身の感覚が改善された。
効果なし…
生化学的測定指標と患者自身の感覚共に改善がなし、あるいは悪化した。
(2)臨床効果の分析(別表参考)
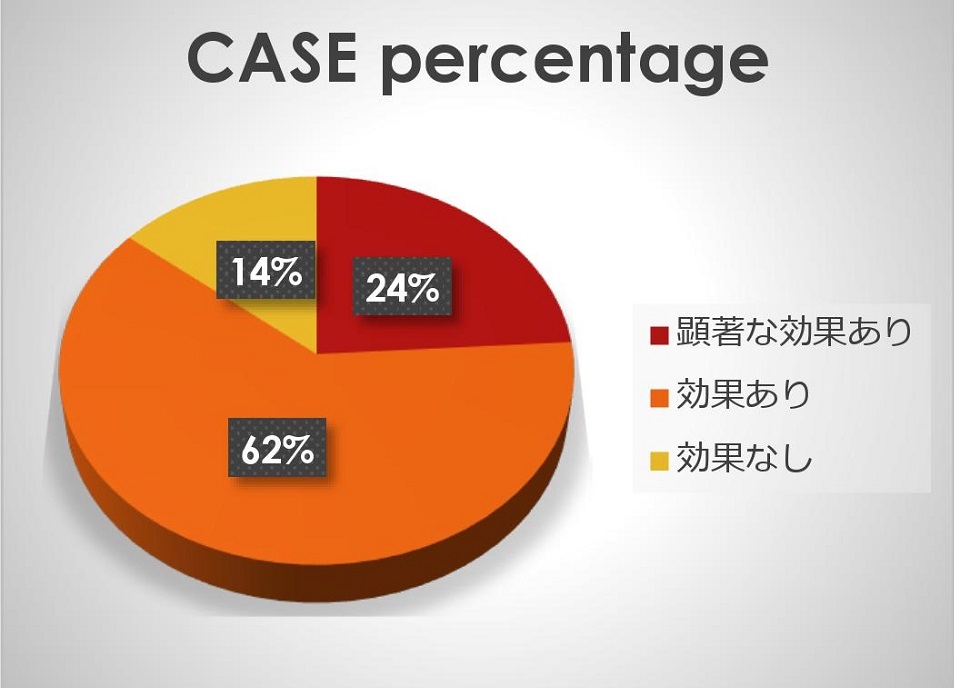
100 人の患者を臨床試験した結果、顕著な効果があったのは 24 人(全体の 24%)である。
効果ありは 62 人(全体の 62%)。したがって有効率は 86%となる。
効果がなかったのは 14 人(全体の 14%)である。
(表1 を参照)
統計学分析(t分析)によって、検体A服用前後の静脈血糖と糖化ヘモグロビンには大きな改善があった(P<0.01)。コレステロールとグリセリン(TG:Trinitrate glyceryl)も改善したが(P>0.05)大きな差はない。
(表 2 を参照)
第二群の総有効率は第一群より高かった。しかし U=1.1529、P>0.05。従い、二群の比較差異なし。
第二群の顕著な有効率は第一群より高かった、且つ U=2.8095、P<0.01。従い、第二群の治療効果は第一群より良かった。
第二群の無効率は第一群より低かった、且つ U=2.0544、P<0.01。従い、第二群の治療効果は第一群より良かった。
第二群の有効率は第一群より高かった、しかし U=1.648、P>0.05。従って二群の比較差異なし。以上の分析により、検体Aの服用量は、毎日 15cc から 17.5cc で一回の服用量は 3.0cc カラ 3.5cc が良いと思われる。
(表 3 参照)
8 週間治療及び 16 週間治療の結果は、有効率がそれぞれ 84%と 88%である。検体Aを二つの治療プロセスにした場合は、16 週間治療の方が有効率は若干高かった。しかし、Ridit の分析により、U=0.55、P>0.05。従って、二群の治療効果には、顕著な差異はない。
(表 4 参照)
表 5 により…
ア.検体Aを 1 プロセス飲用又は、2 プロセス飲用の場合、どちらも静脈血糖値及び糖化ヘモグロビンに対して、著しい降下作用がある。
イ.検体Aを 2 プロセス飲用の結果、静脈血糖値に対して降下効果 P<0.001;検体Aを 1 プロセス飲用の結果、静脈血糖値に対して降下効果 P<0.01。従って、2 プロセスの治療による生化学指標の回復がより高かった。
ウ.第 2 プロセス完了時と完了後 1 ヶ月の血糖値、糖化ヘモグロビン(HbA1c)の比較結果、P
>0.05、差異なし且つ臨床症状安定。
(表 6 参照)
5.結論
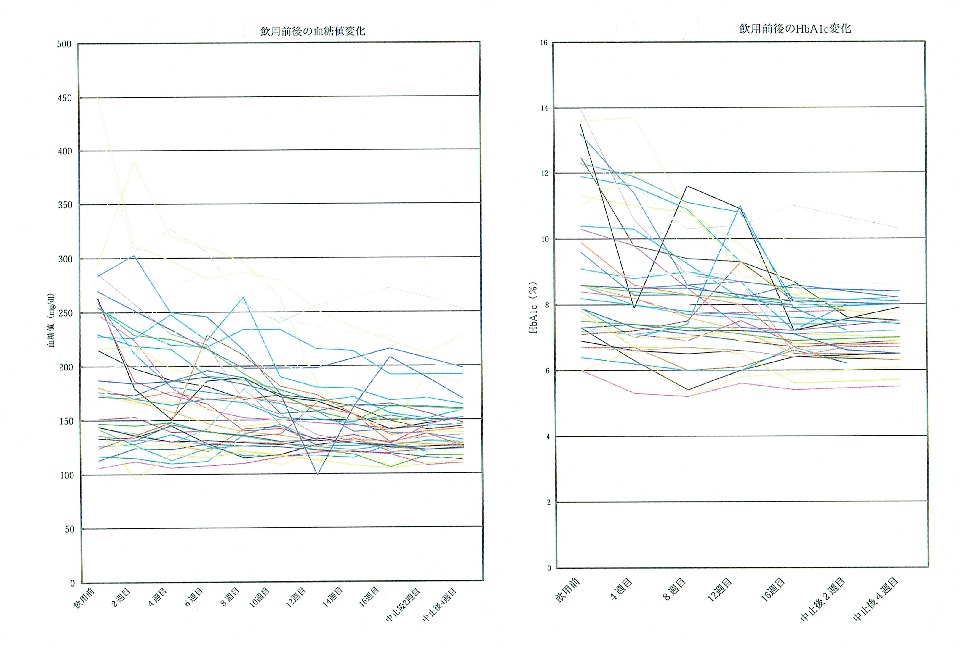
(1)検体Aの血糖値及び糖化ヘモグロビンに対する影響
本臨床報告により、降糖薬物を使用している糖尿病患者に対して、検体Aを同時に飲用すると、良好な降糖効果があることが分かった。
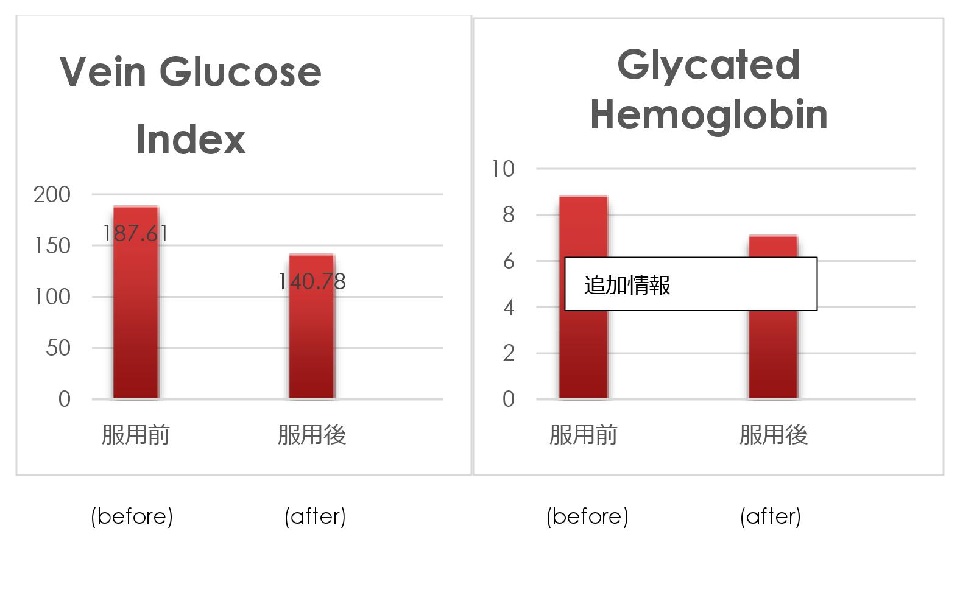
100 例の患者に対しての臨床試験によると、平均血糖値は、飲用前の 187.61±71.62 から、飲用後の 140.38±31.7935 まで低下し(P<0.01)、差異が大きい。糖化ヘモグロビン値(HbA1c)の平均値も、飲用前の 8.785±3.129 から飲用後の 7.077±1.020 まで低下し(P<0.01)、これも差異が大きい。
これらは、検体A自体がもつ降糖効果か、あるいは検体Aが既存の降糖薬物の治療効果を高めた結果によるものなのか、さらに一歩進めた研究が必要であろう。
(2)検体Aのコレステロールに対する影響
糖尿病で高血脂(コレステロール)を合併症として有している患者は、検体Aを飲用した後にコレステロール値とグリセリン値に一定の改善が見られた。統計学的処理を行った結果(P<0.05)と、大きな差異がないことが分かった。
(3)検体Aの一日の服用量
今回の試験では毎日の服用量によって二群の観察を行った。
第 1 群は、毎日 7.5cc から 8.75cc の服用量で 50 例を観察した。第 2 群は、毎日 15cc から 17.5cc の服用量で 50 例を観察した。
有効率は、第 2 群の方は第 1 群よりやや高かった。但し、P>0.05 なので二群の差異は大きいとは言えない。
「顕著な効果あり」及び「効果無し」のデータを見れば、第 2 群は第 1 群より著しく良好、且つ
P<0.01 である。従って、検体Aの服用量は毎日 15cc から 17.5cc が最適と判断できる。
(4)検体Aを用いた治療プロセスに関する研究
検体Aを 8 週間連続飲用することを 1 治療プロセスとする。
連続 16 週間飲用することを 2 治療プロセスとする。
1 治療プロセス及び 2 治療プロセスをそれぞれ 50 例の患者らで観察した。臨床観察の有効率は、それぞれ 84%と 88%となった。U=0.54、P>0.05 だったので二組の差異はなかった。
治療プロセスと有効率の関係を更に検討するため、上述二組の生化学指標について対象研究を行った(詳しい内容は表 5 を参照)。
表 5 のデータによると、二組共に良い治療効果が確認できた。が 2 治療プロセスを受けた患者らが、より良い結果を得られたことが分かった。これは、前述の有効率の話と食い違いがあったが、治療プロセスと治療効果にかけられる要因については、更なる研究が必要と思われる。
(5)追跡観察の結果に対する意見
表 6 の結果によると、検体Aの飲用を停止した 1 ヶ月後も生化学指標は元に戻らなかった。また、患者自身の感覚も変わりがなかった。
この短期効果は以下のことを示している:
検体Aは人体機能における体質改善、免疫力の増強及び糖尿病治療中の効果安定などの面で大いに効果がある。
(6)糖尿病患者に対する有効的保健品
試験を行った 100 例の糖尿病患者のうち、顕著な効果があらわれたのは 24 例、効果がありと示されたのは 62 例であり、併せて総有効率は全体の 86%であった。
これらの患者の検体A服用以前の状態について言えば、種々の生化学的指標は理想に対して必ずしも満足のいくものではなく、加えて自覚症状も良いものではなかった。我々は患者に対して、従来の治療を維持しながら検体Aを服用するという方法をとったが、2 ヶ月間から 5 ヶ月間の観察の結果によって、満足のいく効果が確認できた。
以下に例を挙げる…
南河**** 女性 53 歳 カルテ No,***327 職業:食品工場勤務後退社者
病状:慢性腎臓炎歴 28 年、糖尿病歴 12 年。
全身に浮腫があり、喉が渇き、多食、脱力感、一日中倦怠感がある。
【患者の治療歴】…
漢方薬と西洋医療の治療をしていたが効果がなく、逆に血糖値が上昇した。
空腹時血糖値は 192ml/dl まで上がっていた。糖化ヘモグロビンも 8.9%まで上がっており、尿糖は+++から++にあった。【検体Aによる治療結果】
我々は従来の治療を行いながら、同時に検体Aを毎日 5 回、毎回 3.0ml から 3.5ml を 2 ヶ月間投与した。
血糖は 192ml/dl⇒184ml/dl⇒167ml/dl⇒144ml/dl⇒110ml/dl と低下し、糖化ヘモグロビンも 8.9%⇒8.2%⇒8.9%⇒7.5%⇒6.5%⇒6.2%と、徐々に低下した。また尿糖に関しても+++から-に変化した。2014 年 12 月 23 日に再び検査を行ったが、
血糖は 94ml/dl、血糖ヘモグロビンは 6.0%、尿糖は(-)と安定している状態であり、腎臓機能を表す生化学機能も改善され、その他の検査も指標値が反転しておらず、患者自らも感覚が良好で満足している。
さらに 100 例の患者に対して、検体Aを投与する前に、投与中及び投与後に関し、腎機能の検査を行ったが、一例の損壊も発見されなかった。よって、検体Aは無毒、無副作用で服用できる保健食品であることを説明できる。
(7) 検体Aの今後の課題
検体Aの臨床試験を通じて言えることは、検体Aは糖尿病において科学的な指標を改善するだけでなく、同時にかかわっている高血圧、尿たんぱく、胃腸機能不全、循環器機能障害などにおいても良好な調節作用があるということである。
例えば、体の痺れ、便秘、腹部膨満、頭痛、肥満などを伴う患者にも、ある程度の改善が確認できた。
これは、検体Aの主成分であるシリカが植物性であることから、原材料であるもみ殻が地中から吸収した豊富な微量栄養素を含んでいることに加え、人体との親和性が良好であることから、各臓器機能を正常へと改善及び維持する機能を有するためと考えられる。また、検体Aによる腸内環境の調節により栄養吸収、排泄物の排出、体質を増強し免疫力の増加をも促し、自身の自然治癒能力によって病気を克服するものであると考えられる。
これらによって我々は、検体Aが心臓及び脳血管病、胃腸病、免疫系統の疾患、腎臓病、癌など成人病に対して、適当な薬物の治療と同様に良好な治療効果があるのではないかと、大胆に予想をすることが出来る。これは検体Aに対して、今後の新しい研究課題でもある。
検体A対糖尿病補助治療作用一覧表
『Vegetable Silica Concentration』-(“V. S. C.”)
Clinical Trial about Efficacy on Diabetes Patients under the Combination Therapy.
1. Clinic:
TOTTO RI UNIVERSITY HOSPITAL-Japan
NISHINOMIYA WATANABE HEART BLOOD VESSEL CENTER-Japan
ARAMOTOTOWN INTERNAL MEDICINE CLINIC-Japan
OZU CLINIC – Japan
OMORI INTERNAL MEDICINE CLINIC-Japan etc
2. Tested Subject :
Subject number:Male 61 Female 39 Total 100
Age :31~81
Diabetes disease duration :2 months ~26 years
Diabetes complications:Coronary Artery disease 29、Hypertention 23、
Brain Vessel disease 22, Kidney disease 8, Peripheral Nerve
Lesion 7
Selected Subjects by Blood Glucose Level :
Measured at fasting time – more than 120mg/dl
Measured at 2 hours after meal - 180mg/dl
3. Test Method : Observation period – 8 weeks
No change of existing Diabetes Medication and Lifestyle so far taken. A) Administration:100cases devided into two groups.
First group:wake-up time、3 between-meals 、before sleep
Dosage 1.5cc ~1.75cc plus water 200cc
Second group: same time above, Dosage 3.0cc~3.5cc+water 200cc
4. Observations
A) Subjective symptoms, Side effects etc to be recorded
B) Measuring Liver & Kidney functions & Glycated hemoglobin blood glucose(HbA1c)- before and after the Test .
Vein blood glucose level at fasting time in every 2 weeks & Urinary Glucose in every 3 days.
5. Results
C) Criterion on Effectiveness
① Remarkable result
Both biochemical index & subjective symptoms were improved a lot
② Significant result
Biochemical index has small improvement while subjective symptoms improved well.
③ No improvement
Neither biochemical index nor subjective symptoms improved.
D) Analysis of Clinical Trial
1) Observation on efficacy with all cases
2)V.S.C.’s Vein Blood Glucose & Glycated Hemoglobin before & after
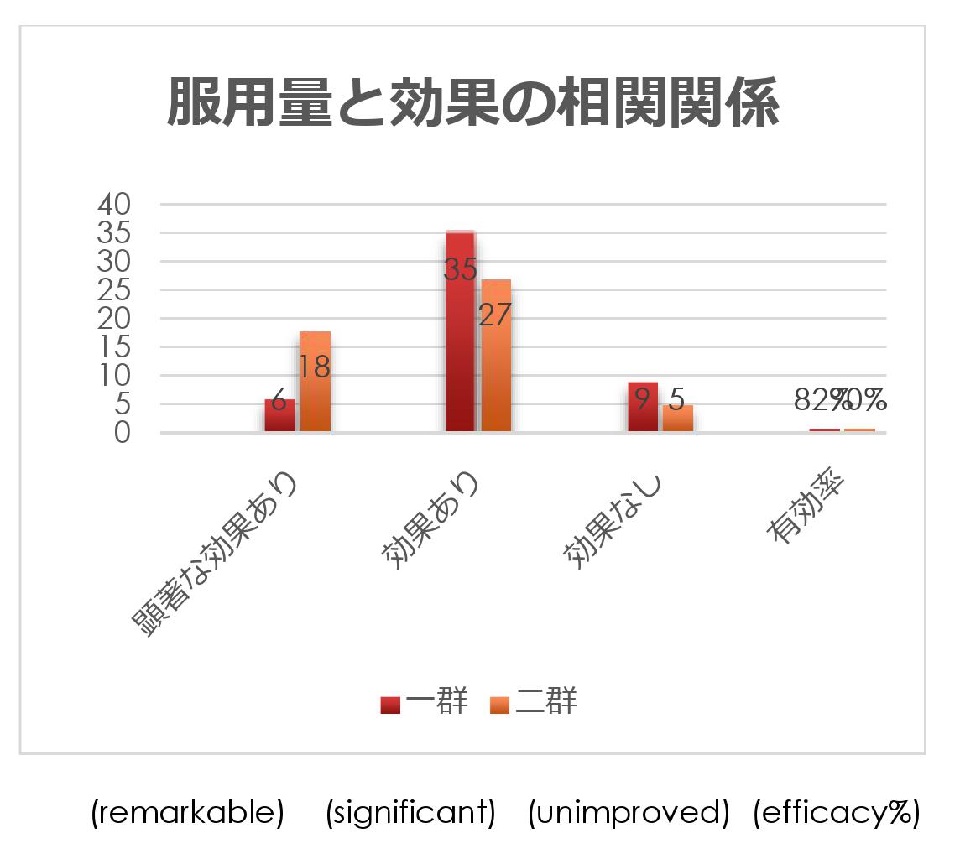
3)Correlation between V.S.C’s dosage and efficacy
Correlation between Dosage and Effiacy (1st group & 2nd group)
6. Summary of the Clinical Trial Result
A) Efficacy of “V.S.C.” upon Blood Glucose and Glycated Hemoglobin
According to the Report of the Clinical Trial, V.S.C. shows obvious performance for lowering vein vessel blood level under the combination therapy with prescription drugs. (blood sugar-lowering medicine) . And no any side-effects were observed.
However, further study is to be done in order to know whether such good results come from the “Effect by V.S.C.” itself or “Synergy effect with prescription drugs” under the combination therapy.
B)Daily intake(dosage) of V.S.C.
1st Group : 7.5cc~8.75cc per day and 50cases observed
2nd Group : 15cc~17.5cc per day and 50 cased observed
Basically, there is no so big difference on efficacy% between 1st and 2nd Group.
However, 2nd Group might have somewhat better result as as to the number of Remarkable’s case and No improvement case.
Consequently, optimum dosage might be considered as 15cc~17.5cc/day.
C) Besides the clinical trial mentioned above, another efficacy test was done with 16 weeks observation period instead of 8 weeks too.
Efficacy % of two test are - 84% in 8 weeks and 88% in 16 weeks.
Longer observation period shows better result.
Follow-up observation also done until 1 month from the date of termination of V.S.C. dose. No unfavorable side-effect nor influence observed on the tested subjects and no change with biochemical index, subjective symptoms etc.
In terms of physical work ability, internal body reform, enhancement of immunity and improvement for ethical medication of Diabetes, greater effectiveness are proved to be clarified.
D) Conclusion for Efficacy upon Diabetes Patients
Among 100 Diabetes patients, 24 cases with remarkable and 62 case with significant, then totally 86% are regarded as effective results.
Most of all patients’ biochemical index and subjective symptoms were not satisfied status, but 2 months ~ 5 months Clinical Trial of V.S.C. under the combination therapy shows a great performance of Efficacy.
(Remarks)
The name of the product which is sold in Japan –“a specimen”
Website : http://grant.or.jp/mottokaradatengoku/
Contents: 500 ml per one plastic bottle for use of 1-1.5 months period
3 components : 1. Shaff Silica (amorphous) 2. Carrot Saponin extract 3. Inositol The name of the exclusive distributor : KK GRANT, Kobe City, Hyogo Pref., Japan











